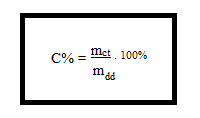Nồng độ phần trăm là gì? Công thức tính nồng độ phần trăm
Trong phần chương cuối của chương trình hóa học lớp 8, các em sẽ được học về chương dung dịch, ở chương này kiến thức và bài tập không quá khó và phức tạp, nhưng đòi hỏi các em cần nắm chắc các kiến thức cơ bản nhất của chương. Hi vọng bài viết này sẽ giúp ích các em trong việc nắm vững lại kiến thức trọng tâm về phần dung dịch này. Nồng độ phần trăm là gì? Công thức tính nồng độ phần trăm
1. Nồng độ phần trăm là gì?
Nồng độ phần trăm của 1 dung dịch là 1 đại lượng cho biết trong 100 gam dung dịch sẽ có bao nhiêu gam chất tan. Nồng độ phần trăm, kí hiệu là C%
2. Công thức tính nồng độ phần trăm
Trong đó:
- C%: nồng độ phần trăm
- mct: khối lượng chất tan
- mdd: khối lượng dung dịch
Mặt khác: mdd = mct + mdm (mdm là khối lượng của dung môi)
– Từ công thức chuẩn trên, ta có thể suy ra được các công thức kèm theo như sau:
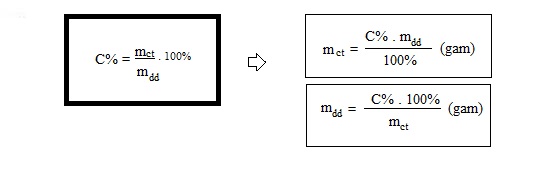
Ví dụ: cho 30 gram muối ăn hòa tan vào trong 90 gram nước, hãy tính nồng độ phần trăm của dung dịch trên.
Hướng dẫn:
Trước tiên, ta tính khối lượng của dung dịch nacl qua công thức:
Mdd= 30 + 90 = 120 (gam)
Sau đó, ta tính nồng độ phần trăm của dung dịch NaCl theo công thức:
C% = m ct / m dd x 100%
=> C% = (30/120) x 100% = 25%.
3. Các bước tính toán để xác định nồng độ phần trăm
Bước 1: đọc kĩ đề và xác định số chất có trong dung dịch (đặc biệt quan tâm đến số dư của các chất tham gia phản ứng)
Bước 2: tìm khối lượng dung dịch sau khi tham gia phản ứng theo công thức đã cho trước đó là:
mdd = khối lượng các chất tan cho vào dung dịch + khối lượng dung môi – khối lượng chất kết tủa – khối lượng chất khí
Bước 3: tìm khối lượng chất tan trong dung dịch để có thể tiến hành tìm nồng độ phần trăm.
Bước 4: tính C% theo công thức tính nồng độ phần trăm
4. Bài tập áp dụng và hướng dẫn giải:
Bài tập 1: xác định nồng độ phần trăm của dung dịch.
Hòa tan hết 20 gam hcl vào trong 40 gam nước. Hãy tính nồng độ phần trăm của dung dịch này.
HD giải:
- Ta có khối lượng dung dịch là: mdd = mct + mdm = 20 + 40 = 60 gam
- Vậy nồng độ phần trăm dung dịch là: C% = (20/40) x 100% = 33,3 %.
- Kết luận: vậy nồng độ dung dịch của NaCl là 33,3%.
Bài tập 2: biến thể 1 của cách tính nồng độ phần trăm.
Bạn hãy tính khối lượng của KCl có trong 200g dung dịch KCl 15%
HD giải:
- Áp dụng công thức c% = (mct/mdd).100% ta có:
- C% = (m KCl / 200) x 100 = 15 (%)
- => m KCl = (15 x 200) / 100 = 30 (gam)
- Kết luận: vậy trong 200g dung dịch KCl 15% có 30 gam KCl
Bài tập 3: biến thể 2 của cách tính nồng độ phần trăm.
Đem hoà tan 40 gam muối vào nước được dung dịch có nồng độ 10%. Hãy:
a) Tính khối lượng dung dịch nước muối thu được
b) Tính khối lượng nước cần dựng cho sự pha chế
HD giải:
a) Áp dụng công thức C% = (mct/mdd).100% ta có:
- mdd = (mmuối x 100)/C% = (40 x 100)/10 = 400 gam
- Kết luận: vậy khối lượng dung dịch a là 400 gam.
b) Áp dụng phương pháp bảo toàn khối lượng, ta có:
mnước= mdd – mmuối = 400 – 40 = 360 gam
Kết luận: vậy để có thể hoàn tan 40 gam muối thì chúng ta phải cần 360 gam nước để tạo ra 400 gam dung dịch.

Từ khóa tìm kiếm google: Nồng độ phần trăm là gì; Công thức tính nồng độ phần trăm; nồng độ % là gì?; tính nồng độ % của dung dịch;
Các bài viết mà bạn cần quan tâm:
Điều chế Clo trong phòng thí nghiệm
Các phản ứng hóa học của Sắt (Fe) và hợp chất quan trọng
Chuyên đề liên kết hóa học lớp 10
Liên hệ: Facebook: Sinhh Quách
Fanpage: PageHoahocthcs
♥Cảm ơn bạn đã xem: Nồng độ phần trăm là gì? Công thức tính nồng độ phần trăm